Flüssigsprengstoffe
- Chemische Struktur
- Chemische und physikalische Eigenschaften: Zustand, Detonationsgeschwindigkeit, brisance (die Brisanz einer hochexplosiven)
- Die Empfindlichkeit des Materials zu Beginn (Klassifizierung basiert auf Sicherheitserwägungen)
- Der Sprengstoff zivile und militärische Anwendungen
Diese Bewertung wird sich auf die chemischen und physikalischen Eigenschaften von Flüssigsprengstoffen (eine explosive Substanz oder mehr, wenn sie mit einer Mischung zu tun), und die wichtigsten Anwendungen, bei denen verschiedene flüssige Sprengstoffe verwendet werden.
Explosive kann entweder von einer oder mehreren Substanzen hergestellt werden. Flüssigsprengstoffe, ähnlich wie bei allen anderen Sprengstoffe werden in einem metastabilen Zustand, so dass (unter geeigneten Bedingungen), um das Auftreten einer schnellen chemischen Reaktion, ohne dass die Gegenwart eines Umwelt Reaktant, wie Sauerstoff gefunden. Flüssigsprengstoffe können durch mechanische Schlag, Reibung oder Wärme initiiert werden.
Die Entwicklung von Flüssigsprengstoffen und deren Verwendung
Die erste flüssige Sprengstoff, Nitroglyzerin, wurde im Jahr 1846 von einem italienischen Chemiker namens Ascanio Sobrero erfunden, die mit einer Lösung, die Salpetersäure und Schwefelsäure nitriert Glycerin. Diese Substanz, aus der Nitroester Familie, erheblich erweitert das Spektrum der Anwendungen, bei denen Sprengstoffe verwendet werden könnten, neue Anwendungen bisher nur serviert von Schwarzpulver enthalten.
Die sichere Herstellung und der Transport von Nitroglyzerin war problematisch; Im Laufe der Jahre nahm sie das Leben vieler. Wenn Nitroglyzerin transportiert, werden kleine Blasen erzeugt, die dann zusammengedrückt werden, wenn die Substanz in Bewegung ist. Diese Kompression führt zu einem lokalen, momentanen Anstieg der Temperatur und den Druck, was zu einer Detonation, auch wenn die Bewegung gering ist.
Viele potentielle Wege zur Überwindung dieses Problems untersucht wurden, bevor eine Lösung im Jahr 1860 von Alfred Nobel wurde gefunden: Nitroglyzerin mit einer festen Substanz mischt, die sie aufnimmt. Diese Mischung, die enthält Nitroglyzerin und einen Kaisal Gohr-Ton wird Dynamit genannt.
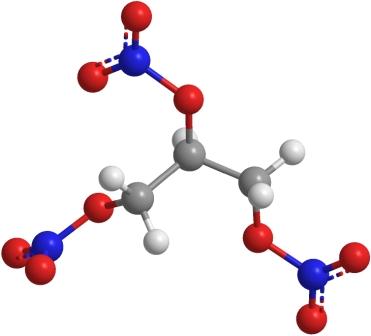
Nitroglyzerin chemische Struktur
- Aussehen: eine ölige, klare Flüssigkeit, oft gelblich
- Summenformel: C3 H5 N3 O9
- Molekulargewicht: 227,1 g / mol
- Sauerstoffbilanz: + 3,5%
- Volumen der gasförmigen Detonationsprodukte: 716 Liter / kg
- Dichte: 1,59 g / cm³
- Schmelzpunkt: + 13,2 ° C
Weitere häufig verwendete flüssige Sprengstoffe
Die explosiven Eigenschaften von Nitroglykol (auch als ethylenglycol dinitras bekannt - EGDN) sind ähnlich die von Nitroglyzerin; jedoch ist es mehr als 100-mal mehr flüchtige als Nitroglyzerin und ist 4 mal so löslich. Da Nitroglycol des Dampfdruck viel höher als Nitroglyzerin ist, kann es eine relativ begrenzte Anzahl von Anwendungen dienen. Es ist weniger viskos als Nitroglyzerin und kann die Geschwindigkeit der Nitrozellulose-basierten Gelatine-Herstellungsverfahren beschleunigen. Mischen Nitroglycol zusammen mit Nitroglyzerin in verschiedenen dynamites ermöglicht die Dynamit-basierten Sprengstoffe in kaltem Klima Ländern, bei niedrigeren Temperaturen, bei denen Nitroglyzerin gefriert und unsicher ist. Ähnlich wie bei anderen Nitroester, Nitroglycol wirkt sich auch auf die Blutzirkulation; Folglich Exposition gegen es ist unsicher, es sei denn seine Konzentration niedrig ist
Chemische Struktur eines Moleküls Nitroglycol
- Aussehen: eine ölige, klare Flüssigkeit, oft gelblich
- Summenformel: C 2 H 4 N 2 O 6
- Molekulargewicht: 152,1 g / mol
- Sauerstoffbilanz: 0%
- Volumen der gasförmigen Detonationsprodukte: 738 Liter / kg
- Dichte: 1,48 g / cm³
- Schmelzpunkt: -20 ° C
- Flammpunkt: 217 ° C
Methylnitrat ist das Produkt aus der Methanol Nitrierverfahren bei dem eine Mischung von nitrosen und Sulfat Säuren verwendet werden. Es kann auch durch Destillation aus einer Mischung aus salpetriger Säure und Methanol hergestellt werden. Methylnitrat ist flüchtig und ist etwa so stark wie Nitroglyzerin. Es wurde als ein flüssiges Treibmittel in der Vergangenheit verwendet, bevor mit stabilen, sicheren Substanzen ersetzt.
Chemische Struktur eines Methylnitrat Molekül
- Aussehen: klare Flüssigkeit
- Molekülformel: CH3 NO3
- Molekulargewicht: 77,0 g / mol
- Sauerstoffbilanz: -10,4%
- Volumen der gasförmigen Detonationsprodukte: 873 Liter / kg
- Dichte: 1,22 g / cm³
Nitromethan wurde 1872 für eine Vielzahl von chemischen Anwendungen entwickelt, einschließlich als Lösungsmittel in chemischen Reaktionen zu dienen, als Bestandteil von Waschmitteln, als Stabilisator in chemischen Verbindungen und auch als Brennstoff für Rennwagen. Es war nicht flüchtig in seiner reinen Form, bis die 1950er Jahre in Betracht gezogen, wenn zahlreiche Unfälle ereigneten sich, wie es transportiert wurde.
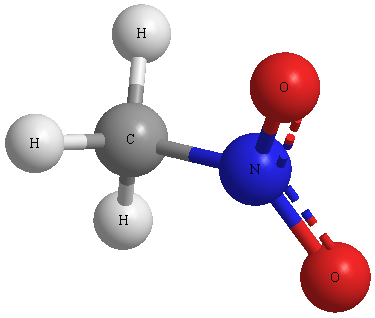
Chemische Struktur eines Moleküls nitromethan
- Aussehen: klare Flüssigkeit
- Summenformel: CH3 NO2
- Molekulargewicht: 61,0 g / mol
- Sauerstoffbilanz: -39,3%
- Volumen der gasförmigen Detonationsprodukte: 1,060 Liter / kg
- Dichte: 1,14 g / cm³
- Detonationsgeschwindigkeit: 6.300 m / sec (bei beschränkt)
Chemische Struktur eines Moleküls Wasserstoffperoxid

Wasserstoffperoxid simulant
Mischungen von Oxidantien und Hydrazin - Astro A und G Astro Sprengstoffe
Aussehen: klare Flüssigkeit
Volumen der gasförmigen Detonationsprodukte: 1.112 Liter / kg
Dichte: 1,36 g / cm³
Detonationsgeschwindigkeit:
- Astrolite A: 7,800 m / sec
- Astro G: 8.600 m / sec
Mischungen aus Wasserstoffperoxid und organischen Stoffen
Mit Wasserstoffperoxid in Mischungen, als Oxidationsmittel zu wirken, mit verschiedenen organischen Materialien hat, führte zu der Entwicklung von verschiedenen Typen von Sprengstoffen und Treibmitteln mit einem höheren Energieinhalt als die Energie aus der Detonation von reinem Wasserstoffperoxid führt. Beispiele für Mischungen können in einer Vielzahl von Patenten gefunden werden, in denen Wasserstoffperoxid mit gemischt wird, beispielsweise Mehl, Sägemehl, Wasser, Glycerin, Ammoniumnitrat und mehr.
Beispiele solcher Mischungen umfassen:
Wasserstoffperoxid in einer Konzentration von 60% -90%, Sägemehl, Harz und ein Geliermittel (Stärke oder Agar-Agar).
Niedrige Konzentration von Wasserstoffperoxid, Glycerin und Wasser.
Wasserstoffperoxid bei niedrigen oder hohen Konzentrationen, Hydrazin und Wasser zu Sprengstoffen reich an gasförmigen Detonationsprodukte herzustellen.
Wasserstoffperoxid, Ammoniumnitrat und Wasser.
Im Jahr 1945, ein Amerikaner namens Ed Laurence gelungen, die explosive Performance und chemische Stabilität von Nitromethan zu verbessern, indem es mit chemischen Substanzen, die zu der Amin Familie kombinieren. Weitere Entwicklungen umfassen Kombinationen wie beispielsweise Aluminium Ammoniumnitrat mit verschiedenen Säuren.
Im Prinzip kann jedes Amin verwendet werden, um einen Nitromethan Sprengstoff herzustellen; Jedoch werden die besten Ergebnisse erzielt, wenn aliphatische verwenden, und nicht die aromatischen Amine. Die empfohlenen Amine schließen Ethylendiamin-Morpholin, diethlaminoethanol; und Anilin- und Tetraethylenpentamin.
PLX, die für die Fernzündung von Landminen in der Vergangenheit verwendet wurden, wird durch die Kombination von 95% Nitromethan mit 5% Ethylendiamin hergestellt. Zusätzliche Aminderivate sind versucht worden; jedoch hat die oben gefunden worden, das wirksamste Verhältnis für eine explosive Substanz.
Im Jahr 1987 wurde ein Sprengkörper C4 und PLX Kombination wurde verwendet, um die Luft zu sprengen Korean Airline Fluges 858. Das Gerät an Bord von nordkoreanischen Agenten ausgeführt.
Diese Gelatinen enthalten, Nitromethan, einem Amin-Derivat, ein Verdickungsstoff und Aluminium.
Beispiele für diese Art von Mischungen umfassen:
- Nitromethan, Nitrocellulose, Ethylendiamin und Aluminiumpulver
- Nitromethan, 38 Benton, Ethylendiamin und Aluminiumpulver
ANNM, Ammoniumnitrat - Nitromethan
Kombinationen von Salpetersäure und organischen Stoffen
Hellhoffites ist eine der ersten Familien umfassen, die mit Flüssigsprengstoffen Dinitrobenzol oder Dinitrochlorbenzol und konzentrierter Salpetersäure vermischt werden. Diese Mischungen wurden weit überwiegend von 1880 bis 1897 verwendet; in späteren Jahren wurde ihre Verwendung aufgrund Stabilität und Sicherheitsprobleme deutlich reduziert. Dinitrobenzol wurde zuerst in einem Prozess 1841 von St. C. Deville synthetisiert, die für das Herstellungsverfahren von TNT (eine Reflexreaktion von Benzol mit konzentriertem Salpetersäure) ähnlich ist. Durch die Veränderung der Verhältnisse von DNB Isomeren (orto, meta, para) und unterschiedlichen Komprimierungsparametern, Mischungen mit der gewünschten Viskosität und Dichte erhalten wurden. Diese sind als Boloron bekannt; sie waren im Einsatz in Österreich nach dem Zweiten Weltkrieg.
Der Hellhoffites wird in den USA unter dem Namen dithekite bekannt; sie enthalten unterschiedliche Verhältnisse von Nitrobenzol und Salpetersäure. Dithekite 13 ist eine spezifische Mischung, die auch die häufigste; die Zahl 13 zeigt den Prozentsatz an Wasser; d.h. dithekite 13 von Salpetersäure / Nitrobenzol / Wasser in einem Verhältnis von 63/24/13 zusammengesetzt.
Oxonites sind noch eine weitere Familie von Mischungen, in denen Pikrinsäure Nitrobenzol ersetzt.
Zusätzliche Mischungen auf Basis von Salpetersäure und organischen Verbindungen wurden im Laufe des 20. Jahrhunderts entwickelt: Während der 1970er Jahre wurde ein Emulsionsgemisch entwickelt von konzentrierter Salpetersäure mit Ammoniumnitrat Mischen und Verbindungen Stabilisierung, was zu gelatinösen Sprengstoffen und stabilen Emulsionen. Die Nachteile dieser Art von Mischungen umfassen ihre korrosiven Eigenschaften, was ihre Lagerung und Verwendung problematisch machen; sowie die Toxizität von Dinitrobenzol.
In der Emulsionssprengstoffe zu Familie gehört das Oxidationsmittel in Form einer wässrigen Lösung in einer Ölphase mit einem Emulgator eingeführt. Diese Substanzen können nach der Zugabe von Gasblasen oder Mikroballons mit einem Zünder ausgelöst werden, während des Herstellungsprozesses. Die wichtigsten Bausteine dieser Explosivstoffe sind Wasser, ein Oxidationsmittel, ein Verdickungsmittel, organisches Material, und im Fall der Kappe empfindliche Sprengstoffs - Gasbläschen oder Mikroballons. Diese Substanzen haben eine gelatinöse pastenartige Textur und andere Additive enthalten, wie beispielsweise Aluminiumpulver.
Substanzen, die zu dieser Familie gehören, die eine gesättigte Ammoniumnitratlösung enthalten, wurden mit dem Ziel der Verbesserung der explosiven Stoffe Beständigkeit gegen Wasser entwickelt. Dies erfolgte durch Zugabe von Wasser zusammen mit sich selbst Mittel zu dem Explosivstoff geliert, wodurch das Erreichen zwei Ziele: Wasser-Proofing es; und die Erhöhung seiner Dichte auf über der Wasserdichte. Diese Verbesserungen ermöglichten diese Sprengstoffe in feuchten Stellen zu verwenden (hauptsächlich Bohrungen in Minen).
Ähnlich wie bei der Emulsion Familie, zündempfindlichen Wasser Geltyp explosive Substanzen können auch hergestellt werden, indem Materialien, wie Monomethylaminnitrat und andere metallische Materialien, Zugabe oder durch Blasen und Mikroballons addieren.
Herr Avi Icar ist der Gründer und CEO von A.S. Explosive Inspection - Service. Er ist ein Ehren Absolvent der Tel Aviv University School of Chemistry, und hat als Offizier in einer Explosive Ordnance Disposal (EOD) Einheit der israelischen Streitkräfte, und anschließend als EOD-Techniker und-Detection-Technologie-Integrator an der Israel Security Agency serviert.