Halb Lives
Wir verwenden integrierte Geschwindigkeitsgesetze und Geschwindigkeitskonstanten Konzentrationen und Zeit zu beziehen. Das Geschwindigkeitsgesetz zu verwenden, hängt von der Gesamtordnung der Reaktion.
Die Gleichungen für Half Lives
Für ein Null-Ordnung reactionA Produkte. Rate = k: t½ = [Ao] / 2k Für eine Reaktion erster Ordnung A-Produkte. Rate = k [A]: t½ = 0,693 / K für eine Reaktion zweiter Ordnung 2A Produkte oder A + B-Produkte (wenn [A] = [B]), Rate = k [A] 2: t½ = 1 / K [Ao ]
Bestimmen eines Half Life
Um eine Halbwertszeit t½ zu bestimmen. die Zeit für die anfängliche Konzentration eines Reaktanden erforderlich ist, um die Hälfte ihres Anfangswertes zu reduzieren, müssen wir wissen:
- Die Reihenfolge der Reaktion oder genügend Informationen, um sie zu bestimmen.
- Die Geschwindigkeitskonstante, k, für die Reaktion oder genügend Informationen, um es zu bestimmen.
- In einigen Fällen müssen wir die anfängliche Konzentration wissen, [Ao]
Ersetzen Sie diese Informationen in die Gleichung für die Halbwertszeit einer Reaktion mit dieser Reihenfolge und lösen für t½. Die Gleichungen sind oben angegeben.
Konvertieren eines Half Life auf eine Geschwindigkeitskonstante
So wandeln wir ein halbes Leben auf eine Rate konstant wissen müssen:
- Die Halbwertszeit der Reaktion t½.
- Die Reihenfolge der Reaktion oder genügend Informationen, um sie zu bestimmen.
- In einigen Fällen müssen wir die anfängliche Konzentration wissen, [Ao]
Ersetzen Sie diese Informationen in die Gleichung für die Halbwertszeit einer Reaktion mit dieser Reihenfolge und lösen für k. Die Gleichungen sind oben angegeben.
Grafische Beziehungen und Half Lives
Wenn wir die Konzentration eines Reaktanden gegenüber der Zeit plotten, können wir die Unterschiede in Halbwertzeiten für Reaktionen verschiedenen Aufträge in den Diagrammen sehen. Wir können einen 0, 1 st identifizieren. oder 2. Ordnung Reaktion aus einem Plan von [A] gegen T durch die Veränderung in der Zeit es braucht, um die Konzentration eines Reaktanden um die Hälfte zu verändern.
Für ein Null-Ordnung reactionA Produkte. Rate = k:
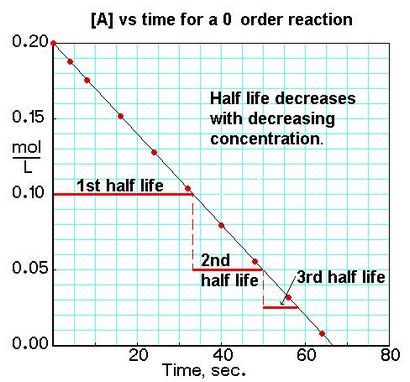
Für eine Reaktion erster Ordnung A Produkte. Rate = k [A]:
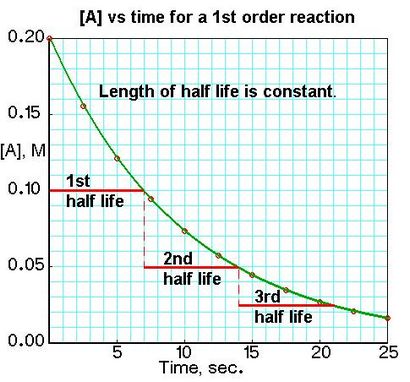
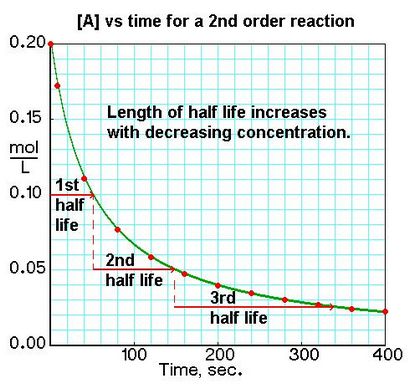
Für eine Reaktion zweiter Ordnung 2A Produkte oder A + B-Produkte (wenn [A] = [B]), Rate = k [A] 2: