Isotopen von Wasserstoff
Eigenschaften der Isotope von Wasserstoff
Wasserstoff hat drei natürlich vorkommenden Isotopen: 1 H (protium), 2 H (Deuterium), 3 H (Tritium). Andere sehr instabiler Kern (4 H bis 7 H) wurde im Labor synthetisiert, sondern tritt in der Natur nicht. Die stabilste Radioisotop von Wasserstoff Tritium, mit einer Halbwertszeit von 12,32 Jahren. Alle schwereren Isotopen sind synthetische und haben eine Halbwertszeit von weniger als einem zeptosecond (10 -21 s). Von diesen ist H 5 am stabilsten, und die am wenigsten stabile Isotop 7H.
Protium, die häufigste Isotop des Wasserstoffs, besteht aus einem Proton und ein Elektron. Einzigartig unter allen stabilen Isotopen, hat es keine Neutronen.
1 H ist die häufigste Wasserstoffisotop mit einer Fülle von mehr als 99,98%. Der Kern dieses Isotops besteht nur aus einer einzigen Proton (Kernladungszahl = Massenzahl = 1) und seine Masse ist 1,007825 amu. Wasserstoff wird im allgemeinen als zweiatomiges Wasserstoffgas H2 gefunden. oder kombiniert mit anderen Atomen in Verbindungen -monoatomic Wasserstoff selten ist. Die H-H-Bindung eines der stärksten Bindungen in der Natur ist, mit einer Bindungsdissoziationsenergie Enthalpie von 435,88 kJ / mol bei 298 K. Als Folge dissoziiert H2 nur in untergeordnetem Ausmaß, bis höhere Temperaturen erreicht werden. Bei 3000 K, ist die Dissoziationsgrad nur 7,85%. Wasserstoffatome sind so reaktiv, dass sie mit fast allen Elementen kombinieren.
2 H oder Deuterium (D), sind die anderen stabilen Isotop von Wasserstoff. Es hat eine natürliche Fülle von
Die häufigste Verwendung für Deuterium ist in der Kernresonanzspektroskopie. Als Kernspinresonanz (NMR) Verbindungen von Interesse erfordert in Lösung aufgelöst werden. die Lösung Signal sollte in der Analyse nicht registrieren. Wie NMR die Kernspins der Wasserstoffatome analysiert wird die verschiedenen Kernspineigenschaft von Deuterium nicht durch das Instrument NMR ‚gesehen‘, deuterierten Lösungsmitteln sehr wünschenswert wegen des Fehlens von Lösungsmittel-Signalinterferenz zu machen.
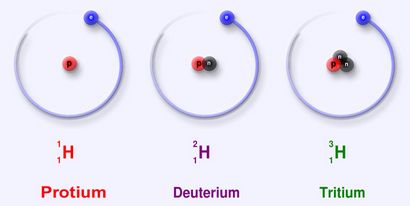
Isotopen von Wasserstoff
Die drei natürlich vorkommenden Isotope von Wasserstoff.