Wie berechnet die formale Ladung von CoCl 2, Sciencing
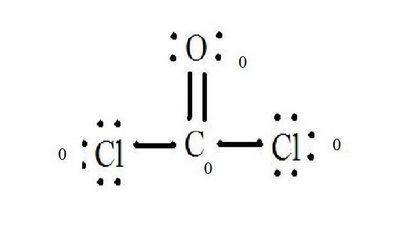
Wenn die formale Ladung eines Moleküls wie CoCl 2 (Phosgen-Gas) zu bestimmen, müssen Sie für jedes Atom und der Lewis-Struktur des Moleküls, die Anzahl der Valenzelektronen kennen.
Valenzelektronenzahl
Schauen jedes Atom in dem Periodensystem der Elemente, um die Anzahl der Valenzelektronen zu bestimmen.
Denken Sie daran, dass zwei Elektronen in der ersten Schale s gehen, zwei Elektronen in der zweiten Schale s, sechs Elektronen in der ersten p-Shell usw. Zur Erinnerung: 1s (^ 2) 2S (^ 2) 2P (^ 6) 3S ( ^ 2) 3P (^ 6)
Passen Sie für Ladung. Wenn das Molekül ein Ion ist, addieren oder subtrahieren, ein oder mehrere Elektronen insgesamt für die endgültige Ladung zu berücksichtigen.
Für CoCl2 (Phosgengas): C = 4; O = 6; Cl = 7. Das Molekül wird nicht ionisiert und hat eine neutrale Ladung. Daher ist die Gesamtmenge an Valenzelektronen 4 + 6 + (7x2) = 24.
Lewis-Struktur
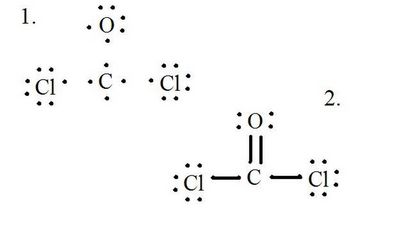
Zeichnen jedes Atom und seine Valenzelektronen, dann Bindungen bilden, wie es erforderlich ist.
Formale Ladung jedes Atom
Zählen Sie die freien Elektronenpaare jedes Atoms in der Lewis-Struktur. Vergeben jedes Atom ein Elektron von jeder Bindung an denen es beteiligt. Fügen Sie diese Zahlen zusammen. In CoCl2: C = 0 Elektronenpaare plus 4 Elektronen von Bindungen = 4 Elektronen. O = 4 Elektronen von einsamen Elektronenpaaren plus 2 Elektronen von Bindungen = 6 Elektronen. Cl = 6 Elektronen von einsamen Elektronenpaaren plus 1 Elektron aus einer Verbindung mit C = 7 Elektronen.

Subtrahiert die Summe aus der Anzahl der Valenzelektronen im ungebundenen Atom. Das Ergebnis ist die formale Ladung für das Atom. In CoCl2: C = 4 Valenzelektronen (V.E.) in ungebundenen Atom minus 4 zugeordnet Elektronen in Lewis-Struktur (L. S.) = 0 formale Ladung O = 6 V. E. - 6 L. S. = 0 formale Ladung Cl = 7 V. E. - 7 L. S. = 0 formale Ladung
Schreibe diese Gebühren neben den Atomen in der Lewis-Struktur. Wenn das Gesamtmolekül eine Ladung aufweist, schließt die Lewis-Struktur in Klammern mit der Ladung außerhalb der Klammern in der oberen rechten Ecke geschrieben.
Berechnen der formale Ladung für Moleküle Übergangsmetalle enthält, kann schwierig sein. Die Anzahl der Valenzelektronen für Übergangsmetalle werden diejenigen außerhalb des Edelgases artigen Kern sein.